热力学第二定律
理想气体卡诺循环
等压,等体热容关系
理想气体的等压,等体热容:
CV=dTdUCP=dTdH
结合理想气体的焓和物态方程:
{H=U+PVPV=nRT得:两边对T求导:结合CV,CP公式:H=U+nRTdTdH=dTdU+nRCP=CV+nR
令γ=CVCP,
CV=γ−1nRCP=γγ−1nR
绝热过程两参量状态方程
由热力学第一定律:dU=δW+δQ,绝热过程δQ=0由{dU=−PdVdU=CVdT得:CVdT+PdV=0对PV=nRT全微分,得:PdV+VdP=nRdT,或:PdV+VdP=CV(γ−1)dT由两式消去CVdT:Vdp+γPdV=0两边同除PV:PdP+γVdV=0解:pVγ=C由PV=nRT可得:{TVγ−1=CTγPγ−1=C
卡诺循环
以理想气体为工作物质,考虑准静态等温过程和准静态绝热过程:
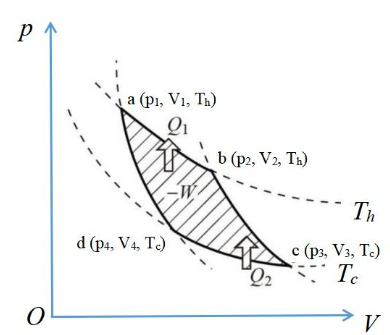
等温线ab,cd: PV=C,平缓 绝热线bc,da:PVγ=C,斜率大
a→b:等温膨胀
Q1=−W1=∫VaVbPadV=RT1∫VaVbVdV=RT1lnVbVa
b→c:绝热膨胀
Q=0
c→d:等温压缩
Q2=RT2lnVdVc
d→a:绝热压缩
Q=0
一轮循环回到初始状态,内能不变。于是对外做功等于吸热:
W=Q1−Q2=RT1lnVaVb−RT2lnV4V3
上式可以化简,对于两绝热过程:
{T1Vbγ−1=T2Vcγ−1T2Vdγ−1=T1Vaγ−1得:VaVb=VdVc于是W=R(T1−T2)lnVaVb
现在定义并计算热机效率:
对于做功机,吸热Q1,放热Q2,做功W。其效率定义为:η=Q1W=RT1lnVaVbR(T1−T2)lnVaVb=1−T1T2(=1−Q1Q2)对于制冷机,在外界做功W下,吸热Q2,放热Q1。其效率定义为:η‘=WQ2=T1−T2T2
热力学第二定律表述
克劳修斯表述:不可能将热量从低温物体传到高温物体而不引起其他变化。(制冷机表述)
开尔文表述:不可能从单一热源吸热使其完全变成有用功而不引起其它变化。(做功机表述)
卡诺定理
所有工作于两个确定温度之间的热机中,可逆热机效率最高。
证明方法是用热力学第二定律的反证法。参考教材P27。
热力学温标
教材P28.有空细看再完善。
克劳修斯不等式
任意热机效率η=1−Q1Q2(定义式)
可逆热机效率η=1−T1T2(理想气体卡诺循环推导)
由卡诺定理,任意热机效率应小于等于可逆热机效率:1−Q1Q2≤1−T1T2变形:T1Q1−T2Q2≤0现在Q1表示吸热,Q2表示放热。为了形式,令Q2也以吸热为正,得T1Q1+T2Q2≤0这是克劳修斯不等式。再推广到n个热源的情形:i=1∑nTiQi≤0n个热源看成一个循环过程中,单一热源n个瞬时贡献δQ,推广到循环积分:∮TδQ≤0
熵
对于可逆循环,∮TδQ=0,
那么对于任意可逆过程的两点A,B,积分∫ABTδQ值相等。(小证明参考p31)
由此定义一个态函数——熵:
SB−SAdS=∫ABTδQ=TδQ
于是我们将热力学第一定律dU=δQ+δW中吸热项也可以用广义力和参量的形式表示:
dU=TdS+i∑Yidyi
现在考虑不可逆过程,(小证明参考p32)
SB−SA≥∫ABTδQdS≥TδQdU≤TdS+i∑Yidyi
不可逆过程作为自然界实际存在的过程,上式视为热力学第二定律的数学形式。
此式不限于系统初态和终态是平衡态,推导方式是将未达到平衡的系统看作多个局域平衡的小部分。
熵增原理:考虑绝热过程,δQ=0,SB−SA≥0 ,把整个自然界看作一个绝热系统,熵永不减小。
自由能
自由能可理解为系统内能可以支配给对外界做功的最大值。
其构造是为了方便判断不可逆过程进行的方向。
亥姆霍兹(Helmholtz)自由能
对于等温过程的系统,
系统从外界吸热:根据热力学第一定律:系统对外做功:引入新的状态函数:于是:系统对外做功最Q≤T(SB−SA)UB−UA=Q+W−W≤(UA−UB)−T(SA−SB)F=U−TS−W≤FA−FB大值不大于其自由能减小
在没有功时,FB−FA≤0,可见等温系统的不可逆过程总是朝着亥姆霍兹自由能减小方向进行。
吉布斯(Gibbs)自由能
对于等温,等压过程的系统,
系统对外界做功:于是:变形:引入新的状态函数:于是:吉布斯−W=p(VB−VA)p(VB−VA)≤FA−FBFB+pVB−(FA+pVA)≤0G=F+pVGB−GA≤0自由能永不增加
可见等温,等压系统的不可逆过程总是朝着吉布斯自由能减小方向进行。
